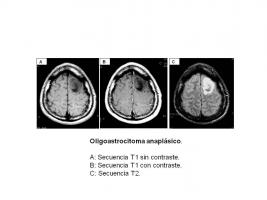
Oligoastrocitoma anaplásico (grado III)
INTRODUCCIÓN
El oligoastrocitoma anaplásico (OAA) pertenece al grupo de los gliomas grado III según la clasificación de la OMS de 2007 (Louis et al; 2007), y se caracteriza por presentar características histopatológicas y moleculares propias tanto de los astrocitomas anaplásicos como de los oligodendrogliomas grado III. La incidencia real de estos tumores es difícil de conocer, pues según diferentes series varía entre un 1,8% a un 19% de todos los gliomas, ya que existe una gran variabilidad entre patólogos experimentados para coincidir en un mismo diagnóstico histológico entre el OAA y el oligodendroglioma anaplásico (ODA).
MANIFESTACIONES CLÍNICAS
La sintomatología de presentación depende de la localización tumoral. Los pacientes pueden presentar cefalea (usualmente matutina), crisis comiciales, síntomas y signos de tracto neurológico largo (alteraciones motoras o sensitivas), alteraciones del campo visual, alteraciones del lenguaje, alteraciones de la memoria, cambio de personalidad, síntomas de hipertensión intracraneal (nauseas, vómitos, papiledema y fotofobia), etc.; sin embargo los síntomas más frecuentes son los tres primeros (DeAngelis; 2001).
La sintomatología de presentación depende de la localización tumoral. Los pacientes pueden presentar cefalea (usualmente matutina), crisis comiciales, síntomas y signos de tracto neurológico largo (alteraciones motoras o sensitivas), alteraciones del campo visual, alteraciones del lenguaje, alteraciones de la memoria, cambio de personalidad, síntomas de hipertensión intracraneal (nauseas, vómitos, papiledema y fotofobia), etc.; sin embargo los síntomas más frecuentes son los tres primeros (DeAngelis; 2001).
NEUROIMAGEN
Como en el ODA, su imagen en RM con gadolinio es heterogénea con necrosis, degeneración quística, hemorragias intratumorales y calcificaciones (visibles mejor en la TAC) [Oligoastrocitoma anaplásico.jpg]. La imagen radiológica en anillo propia del GB, puede representar un peor pronóstico en los pacientes con OAA (Tortosa et al; 2003).
HISTOPATOLOGÍA Y BIOLOGÍA MOLECULAR
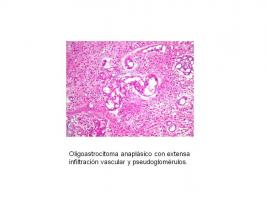
Este grupo de tumores se originan probablemente de una célula glial bipotencial y se caracteriza morfológicamente por un patrón mixto de células de aspecto oligodendroglial entre células de aspecto astrocitario, con signos de malignidad en alguno de los dos componentes [Histopatología Oligoastrocitoma anaplásico.jpg]. La existencia de necrosis obliga a clasificar este tipo de tumores como “GB con componente oligodendroglial” y, por tanto, como un grado IV. Es conveniente identificar la presencia de células oligodendrogliales en un astrocitoma, pues dichos tumores comparten con los oligodendrogliomas la sensibilidad al tratamiento (Cairncross et al; 1994). A nivel molecular son tumores mixtos que comparten características tanto de tumores oligodendrogliales como astrocíticos. Al igual que en el caso del ODA, existen OAAs con y sin pérdida de 1p/19q y también en este tipo de tumores esta co-delección parece implicar un pronóstico más favorable.
Este grupo de tumores se originan probablemente de una célula glial bipotencial y se caracteriza morfológicamente por un patrón mixto de células de aspecto oligodendroglial entre células de aspecto astrocitario, con signos de malignidad en alguno de los dos componentes [Histopatología Oligoastrocitoma anaplásico.jpg]. La existencia de necrosis obliga a clasificar este tipo de tumores como “GB con componente oligodendroglial” y, por tanto, como un grado IV. Es conveniente identificar la presencia de células oligodendrogliales en un astrocitoma, pues dichos tumores comparten con los oligodendrogliomas la sensibilidad al tratamiento (Cairncross et al; 1994). A nivel molecular son tumores mixtos que comparten características tanto de tumores oligodendrogliales como astrocíticos. Al igual que en el caso del ODA, existen OAAs con y sin pérdida de 1p/19q y también en este tipo de tumores esta co-delección parece implicar un pronóstico más favorable.
PRONÓSTICO
La edad de presentación <40a, un buen estado general y la localización frontal son factores clínicos favorables. Desde el punto de vista molecular la presencia de co-delección 1p/19q se ha confirmado como marcador de buen pronóstico en varios ensayos clínicos, entre ellos en el RTOG 9402 (Cairncross et al; 2006) y en el EORTC 26951 (Van den Bent et al; 2006).
TRATAMIENTO
Al igual que en otros subtipos de tumores anaplásicos, hay que tener en cuenta que hasta hace muy poco los ensayos clínicos incluían oligodendrogliomas grado III, oligoastrocitomas grado III, y astrocitomas grado III y grado IV (glioblastoma multiforme) como gliomas malignos. La mayoría de los datos provienen de resultados del análisis por subgrupos de dichos ensayos, y por lo tanto son resultados poco consistentes. El tratamiento del OAA es idéntico al del oligodendroglioma anaplásico [Link a 3.2.4.1.2.2. Oligodendroglioma anaplásico], excepto por la menor quimiosensibilidad objetivada en los OAAs en relación con una menor presencia de co-delección 1p19q en este tipo de tumores y la mayor frecuencia de alteraciones moleculares propias de tumores de estirpe astrocítica.
Al igual que en otros subtipos de tumores anaplásicos, hay que tener en cuenta que hasta hace muy poco los ensayos clínicos incluían oligodendrogliomas grado III, oligoastrocitomas grado III, y astrocitomas grado III y grado IV (glioblastoma multiforme) como gliomas malignos. La mayoría de los datos provienen de resultados del análisis por subgrupos de dichos ensayos, y por lo tanto son resultados poco consistentes. El tratamiento del OAA es idéntico al del oligodendroglioma anaplásico [Link a 3.2.4.1.2.2. Oligodendroglioma anaplásico], excepto por la menor quimiosensibilidad objetivada en los OAAs en relación con una menor presencia de co-delección 1p19q en este tipo de tumores y la mayor frecuencia de alteraciones moleculares propias de tumores de estirpe astrocítica.
BIBLIOGRAFÍA
Cairncross G, Macdonald D, Ludwin S, et al. (1994). Chemotherapy for anaplastic oligodendroglioma. National Cancer Institute of Canada Clinical Trials Group. J Clin Oncol. 12: 2013-2021.
Cairncross G, Berkey B, Shaw E, Jenkins R, Scheithauer B, Brachman D, Buckner J, Fink K, Souhami L, Laperierre N, Mehta M, Curran W. (2006). Phase III trial of chemotherapy plus radiotherapy compared with radiotherapy alone for pure and mixed anaplastic oligodendroglioma: Intergroup Radiation Therapy Oncology Group Trial 9402. J Clin Oncol. 24: 2707-2714.
DeAngelis LM. (2001). Brain tumors. N Engl J Med. 344: 114-123.
Louis D, Ohgaki H, Wiestler O, et al. (2007). The 2007 WHO Classification of Tumours of the Central Nervous System. Acta Neuropathol. 114:97-109.
Tortosa A, Vinolas N, Villa S, et al. (2003). Prognostic implication of clinical, radiologic, and pathologic features in patients with anaplastic gliomas. Cancer. 97:1063-1071.
Van den Bent MJ, Carpentier AF, Brandes AA, Sanson M, Taphoorn MJ, Bernsen HJ, Frenay M, Tijssen CC, Grisold W, Sipos L, Haaxma-Reiche H, Kros JM, van Kouwenhoven MC, Vecht CJ, Allgeier A, Lacombe D, Gorlia T. (2006). Adjuvant procarbazine, lomustine, and vincristine improves progression-free survival but not overall survival in newly diagnosed anaplastic oligodendrogliomas and oligoastrocytomas: a randomized European Organisation for Research and Treatment of Cancer phase III trial. J Clin Oncol. 24: 2715-2722.
- 35267 lecturas