Características fundamentales del ADNmt
El ADNmt está constituido por una doble cadena circular de ADN de 16.569 pares de bases de longitud. Contiene 37 genes que codifican dos ácidos ribonucleicos ribosómicos (ARNr), 22 ARN de transferencia (ARNt) y 13 proteínas que forman parte de cuatro de los cinco complejos que constituyen la cadena de transporte de electrones (siete del complejo I, una del complejo III, cuatro del complejo IV y dos del complejo V). El complejo II, la coenzima Q y el citocromo c están codificados por el ADNn.
Los 37 genes que contiene se disponen unos a continuación de los otros sin nucleótidos intermedios ni intrones. Existe una pequeña región del ADN que no codifica para ningún gen, llamada bucle D, que es donde se localizan los elementos de control para la expresión y replicación del ADN.
[Fig 2. ADN mitocondrial]
Las principales características que rigen la genética mitocondrial son (Di Mauro, 2007):
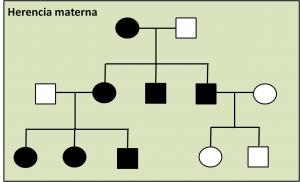
1. Herencia materna.[Fig3. Herencia materna]: En la fertilización, todo el ADNmt procede del oocito. Por tanto, el modo de transmisión del ADNmt y por tanto de sus mutaciones no siguen las leyes mendelianas de herencia (como excepción, las deleciones únicas del ADNmt suelen ser eventos esporádicos, no heredados). Una mujer portadora de una mutación puntual en el ADNmt la transmitirá a todos sus hijos (tanto hombres como mujeres), sin embargo, únicamente las hijas podrán transmitirlo a su descendencia. La existencia en una familia de una enfermedad que afecta a ambos sexos pero donde no hay evidencia de transmisión paterna es altamente sugestiva de una mutación puntual en el ADNmt.
2. Heteroplasmia y efecto umbral. Cada célula contiene de cientos a miles de copias de ADNmt, las cuales se distribuyen de manera aleatoria entre las células hijas en cada división celular. En condiciones normales, todas las copias de ADNmt son idénticas (condición conocida como homoplasmia). Las mutaciones deletéreas afectan generalmente sólo a unas pocas copias de ADNmt en cada célula y tejido en un individuo (heteroplasmia), y la expresión clínica de las mutaciones patogénicas van a depender por tanto de la proporción existente de ADNmt mutado y normal en los diferentes tejidos. En cada órgano o tejido particular es necesaria la presencia de un porcentaje mínimo de ADNmt mutado para producir disfunción mitocondrial (generalmente >80-90%). Este fenómeno se conoce como efecto umbral y es distinto para cada célula y tejido, lo que condiciona una gran variabilidad en la expresión fenotípica de estos trastornos.
3. Segregación mitótica. En cada división celular la proporción de ADNmt en las células hijas puede variar, al ser la distribución de las mitocondrias entre ellas aleatoria, y en consecuencia el fenotipo puede verse modificado. Este fenómeno, conocido como segregación mitótica, explica por qué algunos pacientes con mutaciones en ADNmt pueden presentar distintos fenotipos clínicos a lo largo de la vida. Por ejemplo, niños que sobreviven a un síndrome de Pearson (enfermedad hematopoyética generalmente fatal) pueden desarrollar con los años un síndrome de Kearns-Sayre a medida que las deleciones de su ADNmt descienden en número en sus células sanguíneas (células con un alto índice de replicación) a la vez que aumentan en células postmitóticas del cerebro y el músculo.
4. Alta tasa de mutación. El ADNmt es muy vulnerable y presenta una tasa de mutación espontánea 10-20 veces superior a la del ADNn. En cada individuo se produce a lo largo de la vida una pequeña heterogeneidad en el ADNmt como consecuencia de mutaciones somáticas que se originan continuamente. Esto puede ser debido a la alta producción de radicales de oxígeno que se originan constantemente en la mitocondria y podrían dañar el ADNmt que no está protegido por histonas y donde los mecanismos de reparación parecen ser insuficientes.
Las mitocondrias son ubicuas y por tanto cualquier órgano o tejido puede verse afectado en caso de mutaciones en el ADNmt. Sin embargo, dada la heteroplasmia y el efecto umbral, su expresión fenotípica es altamente variable lo que explica la gran heterogeneidad de los síndromes mitocondriales, incluso dentro de la misma familia.
BIBLIOGRAFÍA
DiMauro S. Mitochondrial DNA medicine. Biosci.Rep. 2007 Jun;27(1-3):5-9.
- 65848 lecturas